CEMIPAI Campus CNRS
1919 Route de Mende
34000 Montpellier
FRANCE
+33 4 34 35 97 50 / 52
contact[at]cemipai.cnrs.fr





Le service de criblage du CEMIPAI est spécialisé dans le test de molécules antivirales. Il est ouvert aux équipes académiques et sociétés privées.
Les expériences sont menées dans les installations de la plateforme par une équipe d’ingénieurs spécialisés dans la manipulation d’agents infectieux de classe 3.
Nos études sont réalisées à façon, avec prise en charge intégrale du projet : réunions préparatoires, réalisation de l’étude, production d’un fichier de données et d’un rapport de résultats
Notre équipe d’ingénieurs possède une vaste expérience dans la découverte d’antiviraux ciblant à la fois les virus et les hôtes, depuis les premières étapes du criblage à moyen débit jusqu’à l’identification et la validation des cibles. Nos tests sont réalisés en microplaques de culture, sur des modèles cellulaires en 2D (monocouches) et 3D (MucilAir™ ). Nos tests sont réalisés sur des échantillons très divers: petites molécules, siRNA, extraits naturels…
Nos services comprennent :
Nous proposons une gamme de tests pour détecter des virus infectieux ou des génomes viraux dans une variété d’échantillons, pour évaluer l’efficacité d’un vaccin ou d’un traitement dans des spécimens animaux ou humains, ainsi que pour aider au développement de nouveaux tests de diagnostic.
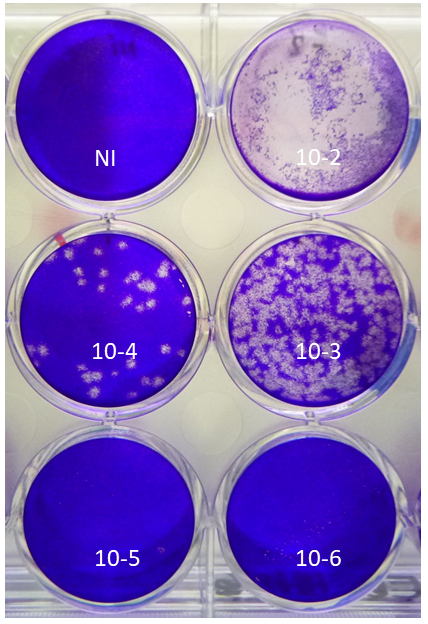
Nos tests comprennent :
Ce service permet de tester, mesurer et comparer les propriétés neutralisantes d’anticorps ou d’échantillons de sérum
Nos tests comprennent :
Ingénieure d’études CNRS

Ingénieure d’études

Ingénieure d’études

Ils/Elles ont criblé sur la PF CEMIPAI Lisa Morichon Grégor Dubois David Bracquemond Sophia Rafasse Mathilde Hénaut
La tarification auditable est disponible ici