CEMIPAI Campus CNRS
1919 Route de Mende
34000 Montpellier
FRANCE
+33 4 34 35 97 50 / 52
contact[at]cemipai.cnrs.fr





Notre service de microscopie NSB3 permet de préparer vos échantillons infectieux pour la microscopie électronique. L’imagerie est réalisé sur le plateau COMET de l’INM à Montpellier.
Prestations 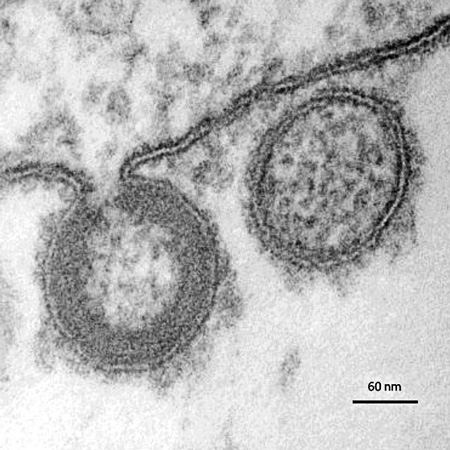
Unique en Europe, notre combiné STED-AFM permet de réaliser en simultané une analyse corrélative par AFM (topographie et imagerie quantitative) et par fluorescence de super-résultion STED. Cet équipement est spécifiquement optimisé pour l’imagerie de pathogènes de classe 3 en conditions natives.
Cellules fixées ou vivantes dans leur milieu de culture, bactéries, levures, macromolécules (acides nucléiques, protéines), polymères, fibres, composites, films lipidiques, vésicules lipidiques (GUV, LUV), vésicules extracellulaires (exosomes), structures biologiques purifiées (capsides virales par exemple), bactériophages, « virus-like particles » et virus de classe 2 et 3. 
BioAFM Nanowizard 4xp (Bruker) spécifiquement modifié pour l’environnement NSB3 avec platine motorisée
Modes d’imagerie à l’air ou en liquide :
XY scan: 100μm x 100μm, Z scan: 15μm
Porte échantillon chauffé de 18°C à 50 ° C, pour boîtes de Pétri de 35x10mm (plastique ou avec fond en verre) ou lamelles de verre de 25 mm.
Incubation C02 pour imagerie cellules vivantes + Injecteur double pompes dans la chambre d’incubation

Objectifs :
Source LED blanche et Epi-Fluorescence Intensilight 100w (Hg, manuel)
Cubes filtres :
Caméra JENOPTIK Fluorescence ProgRes MFcool (2/3 “1.4 MegaPixel CCD, 1350×1024 pixel resolution, 14bit)
Module Confocal / STED – STEDYCON (Abberior)
Détection : 2 couleurs STED et 4 couleurs confocal
Excitation laser : 405 nm, 488 nm, 561 nm, 640 nm
Bandes de détection : 420-480 nm, 505-550 nm, 575-625 nm, 650-700 nm
STED laser : 775 nm (pulsé)
Résolution STED (latéral) 30-40 nm
Champ : jusqu’à 90 µm x 80 µm
Autofocus hardware STEDYFOCUS
Microscope Inversé pour l’imagerie de cellules vivantes en mode TIRF et super-résolution PALM-nSTORM
Notre microscope Nikon Ti-Eclipse est installé en espace confiné L3 pour l’imagerie de cellules vivantes infectées par microscopie de fluorescence à très haute résolution. Ce microscope est équipé d’un bras pour l’imagerie par réflexion totale interne (TIRF, total internal reflection fluorescence microscopy), ou onde évanescente, permettant d’étudier avec une très grande résolution la morphologie ou les évènements intervenant à la membrane plasmique de cellules vivantes.
Equipement : 
Objectifs :
Pilotage avec le logiciel NIS Elements NIKON
Le microscope est installé dans une chambre d’incubation à 37°C pour maintenir la viabilité cellulaire.
Le Celldiscoverer 7 LSM900 Airyscan2 est un système d’imagerie de cellules vivantes automatisé entièrement intégré. Il est installé en espace confiné NSB3 pour l’imagerie de cellules vivantes infectées par microscopie de fluorescence en plein champ ou par imagerie confocale.
Spécificités : 
• Automatisation des acquisitions et pilotage à distance
• Imagerie confocale haute sensibilité grâce aux détecteurs GaAsP et à l’ Airyscan 2
• Imagerie rapide grâce au mode multiplexe
• Résolution augmentée grâce à l’AiryScan 2
• Mode combiné des acquisitions plein-champs et confocales
Equipement :
Objectifs (optique adaptative) :
Illumination BF : contraste brightfield, contraste oblique, contraste de phase adaptatif (PGC)
Fluorescence : unité d’illumination en fluorescence composée de 4 LEDs réparties en 2 unités Colibri
Imagerie Confocale LSM900 avec banc laser diode 405, 488, 561 et 640 nm
Les images confocales peuvent être combinées à une acquisition WF pour ne cibler que la couleur d’intérêt en mode confocal ou en mode SR.
Pilotage avec le logiciel ZEN Blue

 spatial de lumière (SLM) pour générer une grande variété de motifs de faisceaux d’illumination, permettant une illumination optimale pour chaque échantillon et chaque application. Une configuration inversée avec deux objectifs à haute ouverture numérique (un pour l’illumination et un pour la détection), ainsi qu’une chambre d’imagerie entièrement contrôlée sur le plan environnemental, permet des acquisitions à long terme en utilisant une variété de schémas d’illumination.
spatial de lumière (SLM) pour générer une grande variété de motifs de faisceaux d’illumination, permettant une illumination optimale pour chaque échantillon et chaque application. Une configuration inversée avec deux objectifs à haute ouverture numérique (un pour l’illumination et un pour la détection), ainsi qu’une chambre d’imagerie entièrement contrôlée sur le plan environnemental, permet des acquisitions à long terme en utilisant une variété de schémas d’illumination.Lasers : Jusqu’à 5 lignes laser (405, 488, 561, 642 et 685 nm) correction chromatique, jusqu’à 20 filtres d’émission et acquisition bicolore, garantissant un large spectre d’applications.
Objectif de détection : Nikon CFI Apo 25× W à 1,1 NA, immersion eau, avec bague de correction.
Objectif d’illumination : Objectif à immersion eau Special Optics 28,6×, 0,7 NA.
Changeur de grossissement : Grossissements finaux de 31,3× et 62,5× optimisant le champ de vision (FOV) et la taille des pixels.
Détection bi-canal : Deux caméras sCMOS Hamamatsu ORCA Flash, chacune équipée de jusqu’à 10 filtres, séparées par deux miroirs dichroïques sélectionnables
Installés dans l’espace confiné L3, les microscopes du CEMIPAI permettent d’accéder à l’imagerie haute résolution de cellules vivantes infectées ou d’agents pathogènes en milieu natif. Ce plateau d’imagerie L3 est unique en France.
Pour une résolution encore plus poussée, le CEMIPAI propose en parallèle un service de préparation d’échantillons L3 pour la microscopie électronique. Les échantillons sont ensuite observés et analysés en MET sur le plateau d’imagerie COMET à Montpellier.
Ingénieur de Recherche CNRS, PhD

Ingénieure d’études CNRS, PhD

Ingénieur d’études HC Univ. Montpellier
